Les2 - Experimentele controles
Leerdoelen
De student kent / kan :
- Uitleggen waarvoor controles dienen in een experimenteel ontwerp
- Experimentele controles toevoegen aan een experimenteel ontwerp
- Data interpreteren en indien nodig nieuwe controles toevoegen aan het experimenteel ontwerp
Inleiding
In les1 hebben we stappenplan geintroduceerd om een experimenteel ontwerp te maken:
- Welke factor(en) (onafhankelijke variabele) ga je testen?
- Wat zijn de levels van de factor(en)?
- Welke controles moet ik meenemen in het experiment?
- Keuze voor modelsysteem?
- Hoeveel proefobjecten (metingen) per experimentele groep?
- Hoe worden de proefobjecten verdeeld over de groepen?
- Wat ga ik meten (afhankelijke variabele)?
- Hoe ga je meten: gepaard of ongepaard?
- Welke statistische test om de data te analyseren?
In deze les gaan we punt (3) verder uitwerken.
Geen verschil tussen experimentele condities?
Stel je doet een experiment en je meet geen statistisch significant verschil tussen de controle groep en de behandelde groep. Kan je dan concluderen dat de experimentele behandeling geen (specifiek) effect heeft gehad in de populatie die getest is?
Er zijn meerdere mogelijke verklaringen:
- De behandeling heeft inderdaad geen effect in de populatie die getest is
- het gebruikte modelsysteem is niet geschikt om te meten wat je wilt meten
- De uitvoering van het experiment was niet goed
- meetfout: het apparaat dat gebruikt wordt om te meten werkt niet goed of is niet gekalibreerd
- De steekproeven zijn te klein om een effect statistisch significant aan te tonen
Voordat we kunnen concluderen dat een experimentele behandeling geen effect heeft in de populatie moeten we kunnen uitsluiten dat een experiment niet goed is uitgevoerd in het lab. Dit kan door controles mee te nemen in het experimentele ontwerp. Zonder goede controle condities kan een experiment niet worden geïnterpreteerd en kan een onderzoeksvraag niet worden beantwoord. Het niet meenemen van de juiste controles kan leiden tot een verkeerde conclusie waardoor de verkeerde hypothese wordt aangenomen.
Negatieve controle
De negatieve controle is de experimentele groep die de behandeling niet krijgt. Alle andere condities in vergelijking met de behandelde groep(en) zijn wel hetzelfde. Er zijn verschillende negatieve controles:
- Niet-behandelde controle: het modelsysteem krijgt geen behandeling. Dit is de baseline van het experiment
- Vehicle controle: het modelsysteem wordt behandeld met alleen een “vehicle” of “carrier”. De term “vehicle” / “carrier” verwijst naar de substantie die wordt gebruikt om een experimentele behandeling af te leveren aan cellen, dieren of mensen
Voorbeeld1 vehicle control:
Je voegt verbinding X (1 nM) toe aan longkankercellijn A549 en meet vervolgens de levensvatbaarheid van de cellen. De chemische verbinding is opgelost in DMSO, een veel voorkomend oplosmiddel. DMSO kan van zichzelf ook een effect hebben op de levensvatbaarheid van cellen. Om uit te sluiten dat het effect wat gemeten wordt afkomstig is van DMSO en niet van de chemische verbinding die getest wordt voeg je ook DMSO toe aan de cellen, dus alleen het oplosmiddel. Dit is de vehicle control en deze controle vergelijk je met de niet-behandelde controle. De behandelde groep (met verbinding X) vergelijk je vervolgens met de vehicle controle.
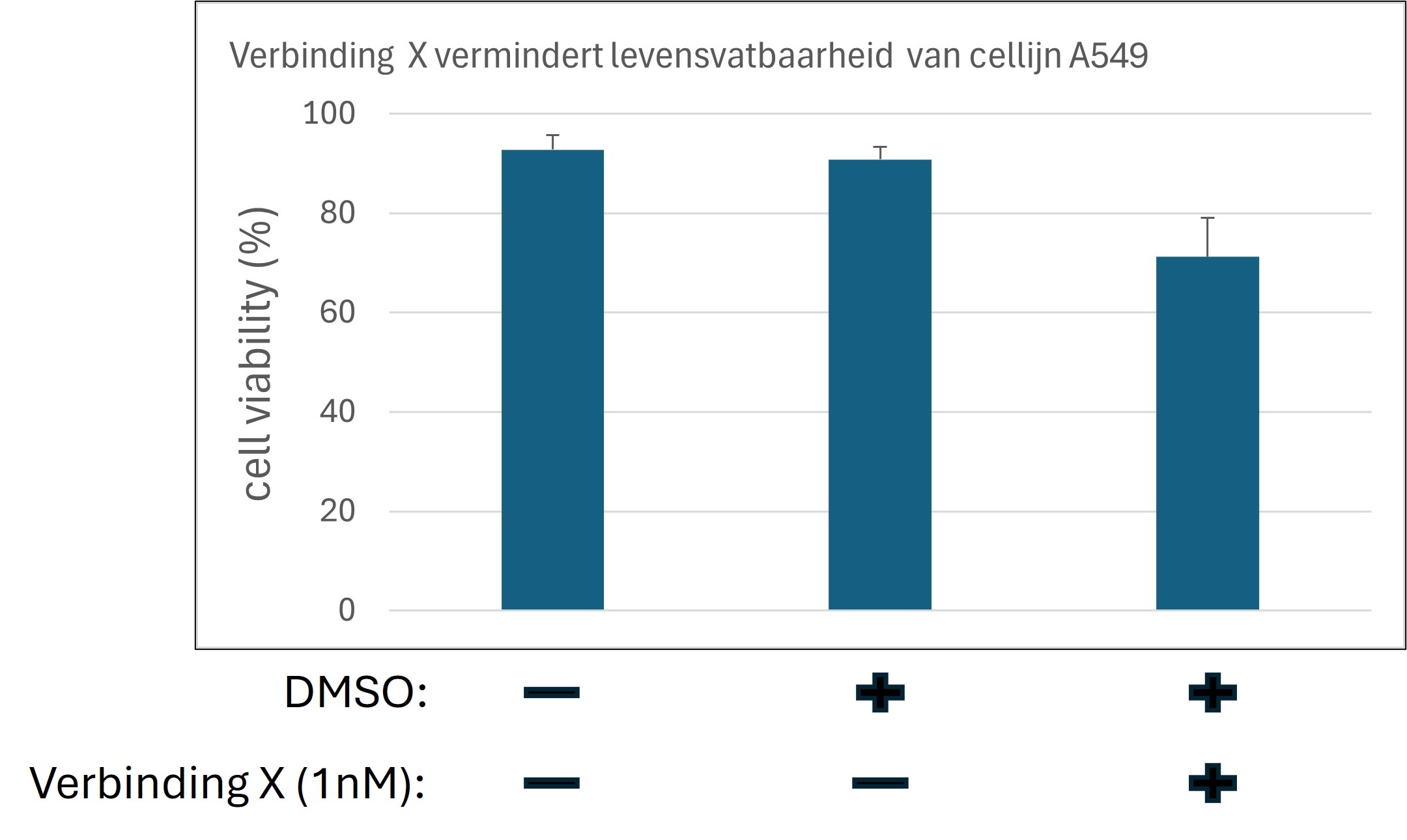
Figure 15: Verwachtte resulaten van blootstelling van cellijn A459 aan verbinding X
In dit voorbeeld verwachten we dat de cellen gezond zijn als ze niet behandeld worden en dat DMSO geen effect heeft op de levensvatbaarheid van de cellen. Na behandeling met verbinding X verwachten we (bijvoorbeeld gebaseerd op eerdere experimenten of wetenschappelijke literatuur) dat er een afname zal zijn in de levensvatbaarheid van de cellen (zie figuur 15).
Deze verwachting kan je vervolgens vergelijken met de resultaten van het lab:
Wat verwacht ik en wat zie ik?
Als dit niet overeenkomt, klopt de hypothese niet of er is iets mis gegaan in het experiment (zie paragraaf over positieve controles).
Het is een goede gewoonte om voor iedere experimentele conditie van te voren te bedenken wat het resultaat is en deze voorspelling te vergelijken met de resultaten van het experiment.
Voorbeeld2, vehicle control:
Overexpressie van MYC is een belangrijke factor bij “small cell lung cancer” (SCLC). MYC speelt in een rol in de ontwikkeling, progressie en de mate van agressie van de kanker cellen. Het veroorzaakt ook mogelijke resistentie tegen geneesmiddelen. Ongeveer 20-30% van de SCLC-tumoren vertoont MYC-amplificatie of -overexpressie. Om de rol van MYC in tumor formatie te bestuderen, gebruik je HEK293 cellen als modelsysteem. Je brengt het MYC oncogen tot overexpressie in HEK293 cellen door middel van een transfectie met een plasmide om het effect op proliferatie te testen (“doubling time).
In dit experiment zijn er twee vehicles: de plasmide die het MYC gen bevat en de transfectiemethode om het plasmide in de cel te krijgen. De negatieve controles zijn dus een transfectie zonder plasmide en een transfectie met de “lege” plasmide (zonder het MYC gen). Om de baseline van de “doubling time” vast te stellen nemen we ook een niet-behandelde control mee. Vanuit de literatuur is bekend dat de “doubling time” van HEK293 cellen ~24 uur is, maar dit hangt af van de groeicondities en passagenumber van de cellen. De verwachtte resulaten staan in figuur 16
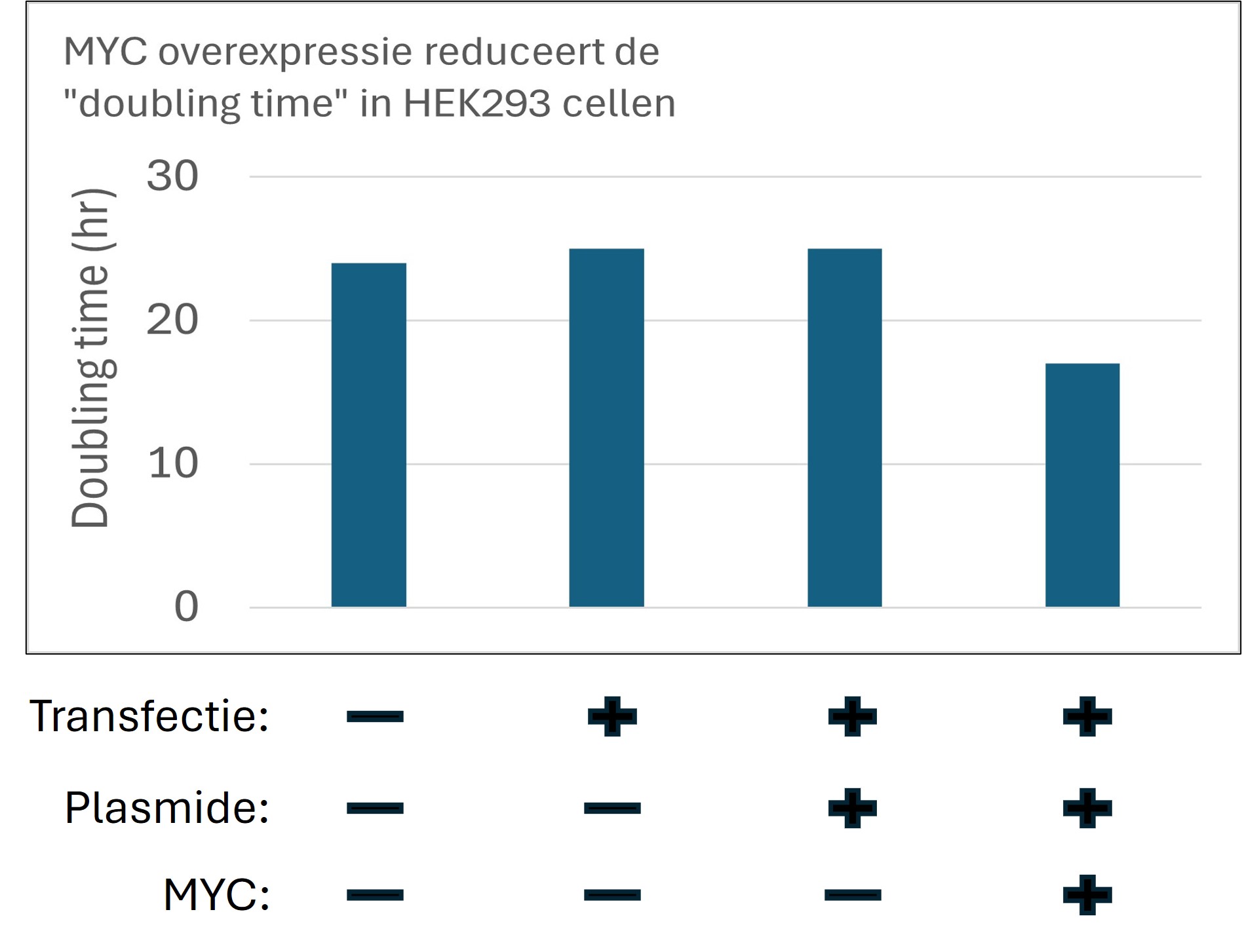
Figure 16: Verwachtte resulaten van overexpressie van MYC op ‘doubling time’ in HEK293 cellen
In dit voorbeeld verwachten we dat de HEK293 cellen een “doubling time” hebben van ~24 uur en dat de transfectie een minimale stress reactie veroorzaken. Dit kan van invloed zijn op de “doubling time” waardoor de cellen iets langzamer gaan delen (“doubling time” wordt groter). De transfectie met de lege plasmide laat geen effect zien op de “doubling time” in vergelijking met alleen de transfectie. Verder verwachten we dat overexpressie van MYC in HEK293 cellen de “doubling time” zal verkorten (de cellen gaan sneller delen).
Als de niet-behandelde controle en de “vehicle” controle herhaaldelijk geen verschil laten zien dan kan in het vervolg één van de twee worden meegenomen in het experimenteel ontwerp. Een experimenteel ontwerp moet altijd een negatieve controle bevatten. Als een negatieve controle ontbreekt is het experiment zinloos en dus een verspilling van tijd, geld en reagentia.
les2_opdracht
Je wilt een (eukaryoot) eiwit produceren met behulp van een E. coli eiwit expressie systeem en vervolgens opzuiveren met een nikkel kolom. Het gen van interesse wordt gekloneerd in een “induceerbare” expressie vector en getransformeerd in de BL21(DE3) E. coli stam. Het eiwit van interesse wordt alleen aangemaakt als de getransformeerde E. coli wordt geinduceerd met IPTG. Dit zorgt ervoor dat de remming in het expressie systeem wegvalt waardoor de bacteriën grote hoeveelheden van het eiwit gaan aanmaken. Na de inductie met IPTG worden de cellen open gebroken en wordt het cell lysaat (met daarin alle eiwitten van de bacterie) opgebracht op een zuiveringskolom die specifiek het eiwit van interesse bindt met behulp van een HIS-tag. Na een aantal wasstappen waarbij alle eiwitten die niet binden worden weggewassen , wordt het resterende eiwit (= eiwit van interesse) los gemaakt van de kolom (elutie) met behulp van een buffer. Het geëlueerde eiwit wordt daarna geanalyseerd met behulp van Western Blot.
Wat is de negatieve controle in dit experiment?
Klik voor het antwoord
Het doel van je experiment is om een eukaryoot eiwit tot expressie te brengen in E. coli en dit vervolgens op te zuiveren. De bacterie maakt ook allerlei eiwitten aan en het is mogelijk dat na de opzuivering er ook vervuiling van bacteriële eiwitten aanwezig is. We willen dus weten wat het achtergrond signaal is na de zuivering. Als negatieve controle gebruiken we E. coli bacteriën die niet geïnduceerd zijn met IPTG. Dit monster bevat alleen maar endogene E. coli eiwitten en als het goed is worden deze allemaal weggewassen van de kolom. Als je na zuivering van de negatieve controle toch eiwitten ziet in de Western Blot analyse weet je dat de wasstappen niet voldoende waren. Het gezuiverde eiwit is gecontamineerd met bacteriële eiwitten.
Bedenk ook goed wat je van te voren verwacht (zie figuur 17).
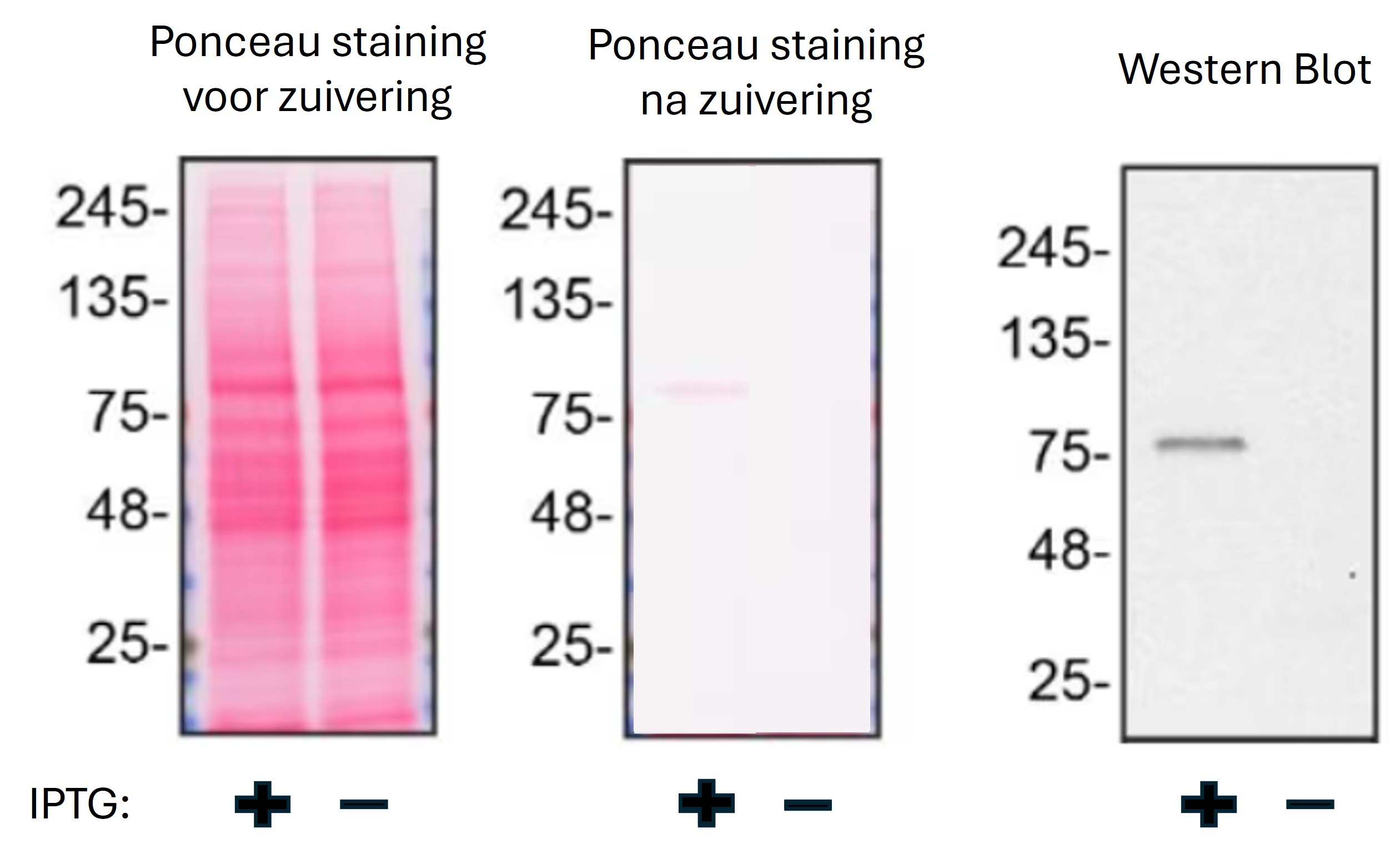
Figure 17: Verwachtte resultaten na eiwitzuivering met een nikkel kolom
Voor zowel de niet-geïnduceerde als de geïnduceerde E. coli bevat het cell lysaat allerlei bacteriële eiwitten (en in de geïnduceerde E. coli nog het extra eukaryote eiwit van interesse). Als de cellysaten voor zuivering worden opgebracht op gel en worden aangekleurd met Ponceau verwachten we een smeer van eiwitten. Als de gezuiverde monsters op gel worden opgebracht en worden aangekleurd met Ponceau verwachten we misschien een specifiek bandje te zien (afhankelijk hoe goed het eiwit tot expressie is gekomen in E. coli). Om te controleren of het gezuiverde bandje het juiste eiwit is wordt het gedetecteerd met een specifiek antilichaam m.b.v. Western Blot analyse.
les2_opdracht
Een onderzoeker test de secretie van TNF\(\alpha\) van twee immunologische cellijnen na blootstelling aan LPS (10 nM). De resultaten staan in figuur 18. De onderzoeker concludeert dat cellijn B een hogere secretie heeft van TNF\(\alpha\) in vergelijking met cellijn A na blootstelling aan LPS (10 nM).
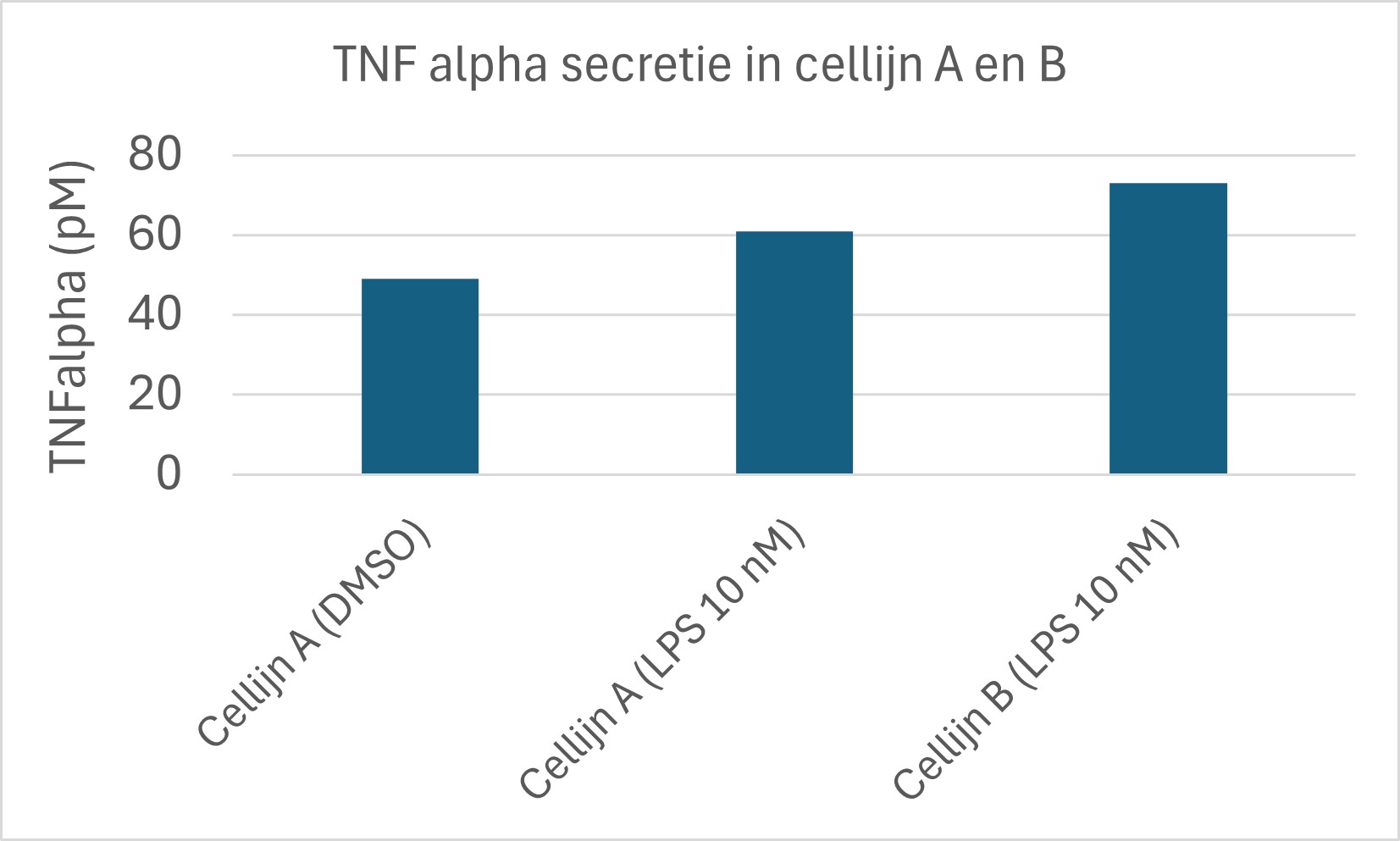
Figure 18: TNFalpha secretie na blootstelling aan LPS
Ben je het eens met de conclusie van de onderzoeker. Waarom wel / niet?
Klik voor het antwoord
De onderzoeker heeft de negatieve controle voor cellijn B niet meegenomen. Als de achtergrondwaarde van cellijn B hoger is dan van cellijn A kan de onderzoeker niet tot de conclusie komen dat TNF\(\alpha\) hoger is in cellijn B in vergelijking met cellijn A
Positieve controle
De positieve controle is de experimentele groep die een behandeling krijgt waarvan je op voorhand weet (vanuit de literatuur of uit eigen ervaring in het lab) dat de behandeling werkt: er is een positief meetresultaat.
Stel dat de experimentele behandeling niet werkt in een experiment. Dan zijn er verschillende verklaringen mogelijk:
- de behandeling werkt niet
- het gebruikte modelsysteem is niet geschikt om te meten wat je wilt meten
- technische fout in de uitvoering van het protocol, bijvoorbeeld:
- je hebt een verouderde oplossing gebruikt
- een enzym dat niet meer werkt
- rekenfout zodat de verkeerde oplossing is gemaakt
- verkeerde oplossing / enzym toegevoegd aan de monsters
- verkeerde incubatie temperatuur
- het monster te lang / te kort geincubeerd
- pipeteerfout
- meetfout: het apparaat dat gebruikt wordt om te meten werkt niet goed of is niet gekalibreerd
- De steekproeven te klein om een statistisch significant effect aan te tonen
Voordat we kunnen concluderen dat een behandeling echt niet werkt (punt 1) moeten we er zeker van zijn dat we alle andere verklaringen zoals beschreven bij punt 3 t/m 5 kunnen uitsluiten. Hiervoor wordt een positieve controle gebruikt. De monsters van de positieve controle worden volgens hetzelfde protocol opgewerkt en gemeten als de andere experimentele condities. Als de positieve controle niet werkt, weet je dat er ergens een fout is gemaakt in de uitvoering van het experiment. Vervolgens moet je achterhalen waar het fout is gegaan in het experiment.
Voorbeeld3, positieve controle:
We gebruiken het experiment zoals beschreven in voorbeeld1. Je test nu verbinding Y op longkankercellijn A549 en test de levensvatbaarheid van de cellen. Je verkrijgt het volgende resultaat (zie figuur 19A)
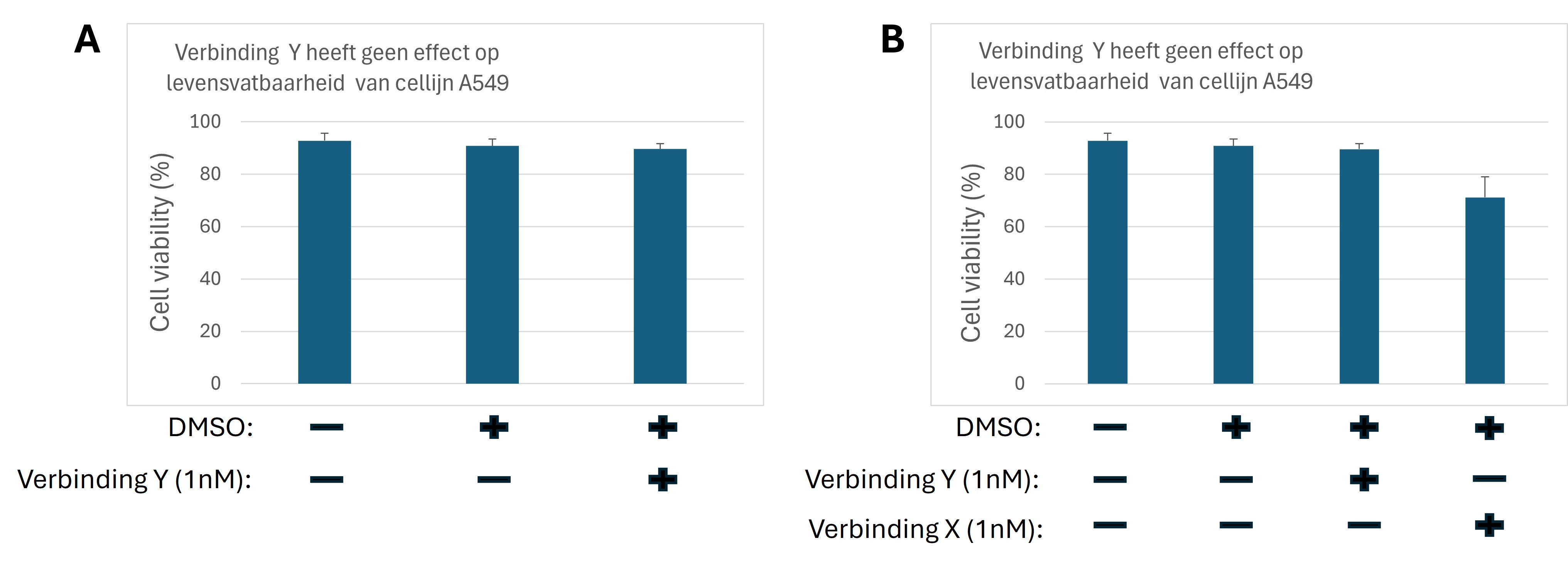
Figure 19: Experiment met en zonder positieve controle
In figuur 19A zien we dat verbinding Y geen effect heeft op de levensvatbaarheid van A549 cellen. Er zijn twee verklaringen:
- Verbinding Y heeft inderdaad geen effect op de levensvatbaarheid van A549 cellen met de geteste concentratie en tijd van blootstelling
- Er is iets verkeerd gegaan in de uitvoering van het experiment. Misschien heb je per ongeluk de verkeerde cellen gebruikt of is er iets verkeerd gegaan tijdens “cell viability assay”
Om onderscheid te maken tussen verklaring (1) en (2) moet er een positieve controle meegenomen worden in het experimenteel ontwerp. Van voorbeeld1 weten we dat verbinding X wel een effect heeft op de levensvatbaarheid van A549 cellen (zie figuur 19B). Als de positieve controle het verwachtte effect laat zien dan kunnen we concluderen dat verbinding Y geen effect geeft. Een vervolg experiment zou dan kunnen zijn om een concentratiereeks van verbinding Y te testen op A549 cellen.
les2_opdracht
THP-1 cellen, afkomstig van een acute monocytaire leukemie patiënt, kunnen worden gedifferentieerd tot osteoclasten via een tweestapsproces. Eerst worden ze gedifferentiëerd tot macrofaag-achtige cellen door incubatie met phorbol-12-myristaat-13-acetaat (PMA). Vervolgens wordt dit proces voltooid door stimulatie met RANKL en M-CSF, wat resulteert in de vorming van osteoclasten. Osteoclasten hebben meerdere celkernen.
Een onderzoeker voert het differentiatie protocol uit en vindt geen enkele cel met meerdere celkernen. De onderzoeker wil graag weten of het differentiatie protocol in de eerste stap (incubatie met PMA) of tweede stap (incubatie met RANKL en M-CSF) is mislukt. De onderzoeker besluit om na de eerste stap van het differentiatie protocol te testen of de cellen macrofaagachtige eigenschappen hebben met behulp van antilichamen die macrofaag specifieke “cell surface markers” (Cd11b en Cd14) aankleuren in combinatie met flowcytometrie. De onderzoeker neemt een positieve controle mee om te testen of de kleuring met de antilichamen goed werkt.
Welke positieve controle kan de onderzoeker gebruiken voor de flowcytometrie analyse.
Klik voor het antwoord
Een (humane) macrofaag cellijn die beide cell surface markers tot expressie brengt zoals bijvoorbeeld HL-60, K562, KG-1, and U937,
les2_opdracht
Zoek op wat de negatieve en positieve controle zijn in een ligatie reactie?
Zoek op wat de negatieve en positieve controle zijn voor de transformatie reactie van de ligase producten?
Klik voor het antwoord
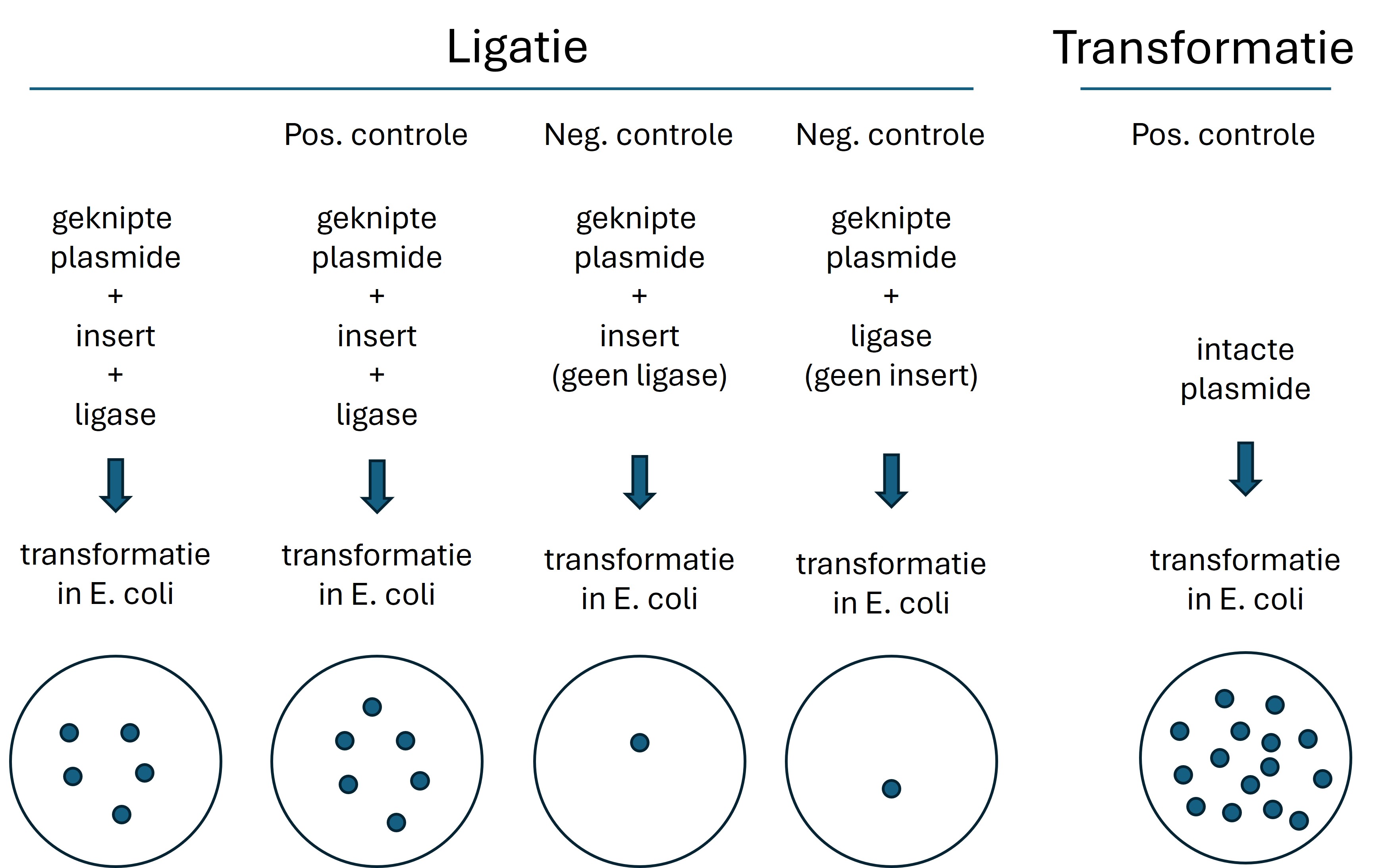
Figure 20: Positieve en negatieve controles in ligatie en transformatie assays
- Het plasmide + insert van de eerste ligatie zijn voor het maken van het nieuwe construct -> kolonies
- Het plasmide + insert van de tweede ligatie (positieve controle) zijn eerder succesvol geligeerd. Controle of de ligatie kit nog goed werkt -> kolonies
- Het plasmide + insert van de derde ligatie (negatieve controle) worden zonder ligase geligeerd. Controle of het plasmide goed geknipt is met restrictie enzymen. Het plasmide moet lineair zijn en niet circulair -> geen of enkele kolonies
- Het plasmide van de vierde ligatie (negatieve controle) wordt zonder insert geligeerd. Controle of het plasmide , zonder insert, aan elkaar geligeerd kan worden -> geen of enkele kolonies
- Transformatie met een intact plasmide. Dit werkt altijd en is een controle of de cellen nog competent zijn voor transformatie -> veel kolonies
Specificiteits controles
Als er een effect wordt waargenomen in de behandelde groep t.o.v. de negatieve controle willen we ook graag weten of dit effect specifiek is voor de behandeling en niet het resultaat is van off-target effecten. Off-target effecten in een experiment zijn ongewenste of onverwachte effecten die optreden doordat een behandeling, stof of genetische manipulatie ook andere moleculen, genen of processen beïnvloedt dan degene waarop het oorspronkelijk gericht is.
Bijvoorbeeld een chemische stof bindt niet alleen aan het eiwit dat je wilt testen (eiwit A) maar ook aan eiwit (eiwit B). Als je een effect waarneemt, wordt het dan veroorzaakt door de interactie van de chemische stof met eiwit A, door de interactie met eiwit B of door de interactie met zowel eiwit A als B. Dit kan leiden tot verwarring over de oorzaak van een waargenomen effect, omdat het resultaat niet uitsluitend toe te schrijven is aan de bedoelde doelwitinteractie. Zonder specificiteit controles kan je de hypothese aannemen dat de chemische stof een effect heeft op eiwit A terwijl het effect in werkelijkheid wordt veroorzaakt door de ongewenste interactie van de chemische stof op eiwit B.
Er zijn veel verschillende soorten specificiteits controles afhankelijk van het type experiment.
Voorbeeld4, specificiteits controle
We gebruiken het experiment zoals beschreven in voorbeeld1. Je voegt verbinding X (1 nM) toe aan longkankercellijn A549 en meet vervolgens de levensvatbaarheid van de cellen. De resultaten van de negatieve controles zijn zoals verwacht dus we concluderen dat verbinding X een effect heeft op de longkankercellijn A549 (zie figuur 25, blauwe balken). De volgende stap in het onderzoek is om te bepalen of deze verbinding specifiek is tegen longkankercellijn A549 of ook een effect heeft op andere kankercellijnen of gezonde longcellen (zie figuur 21, oranje balken). Het laatste is belangrijk want als de verbinding aspecifiek is en een effect heeft op de levensvatbaarheid van verschillende (gezonde) celltypes is het niet geschikt als cytotoxische verbinding in kankertherapie.
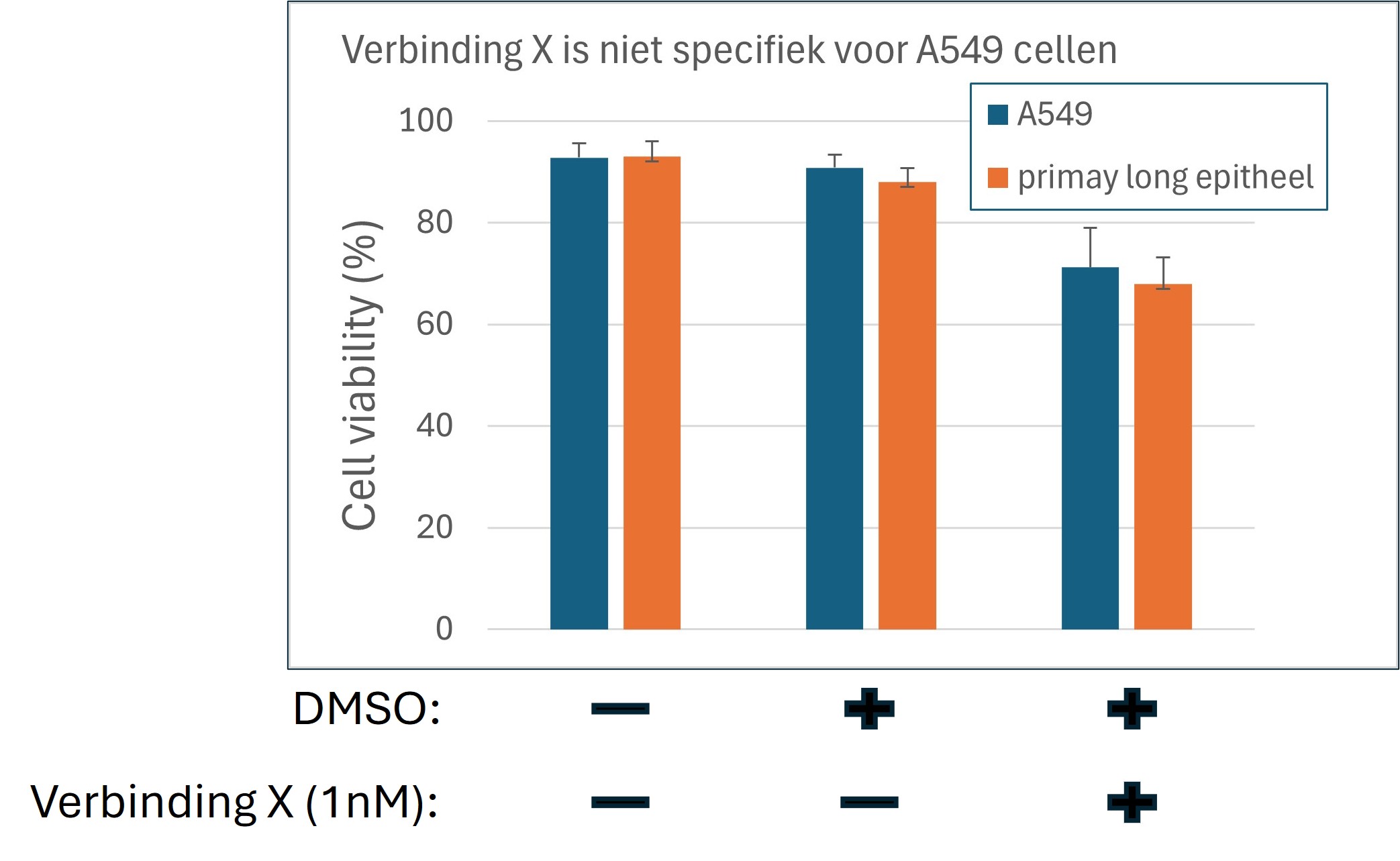
Figure 21: Verbinding X is niet specifiek voor cellijn A549
Voor de oplettende lezer, dit experiment is geen OFAT experiment omdat we nu twee factoren testen:
- Verbinding X (levels: 0 en 10 nM)
- Type cel (levels: A549 en primaire long epitheel cellen)
Dit wordt een multiple factor ontwerp genoemd (zie les4)
Voorbeeld5, specificiteits controle -> scramble control:
Je wilt een knock-out maken van een gen in een bloedstamcel om te testen of dit gen van invloed is op de differentiatie van myeloid cellen. Je gebruikt hiervoor de CRISPR-Cas methode. Het Cas9 eiwit wordt geleid naar een plek in het genoom en maakt daar een dubbelstrengs breuk in het DNA (zie figuur 22). Het DNA wordt vervolgens door de cel gerepareerd en hierbij onstaan fouten zodat er een frameshift mutatie onstaat in het gen waardoor er geen functioneel eiwit afgeschreven kan worden. Om het Cas9 eiwit precies op de juiste plek in het genoom te gidsen, wordt er gebruikt gemaakt van een guideRNA. Het guideRNA bevat een nucleotiden sequentie van 20 bp die complementair is met de genoom sequentie waar het Cas9 eiwit de dubbelstrengs knip moet plaatsen.
](images/les2/22_les2_crispr_cas.jpg)
Figure 22: CRISPR-Cas9
Als specificiteits controle gebruiken we dezelfde guideRNA maar de nucleotide volgorde wordt door elkaar gehusseld zodat de lengte en de CG content hetzelfde blijven maar het niet gericht is tegen een specifieke DNA sequentie. Met een scramble controle kunnen we aantonen dat de effecten die worden gemeten worden veroorzaakt door het speficieke guide RNA en niet door de transfectie procedure en of het inbrengen van vreemd RNA. Dit activeert cellulaire verdedigingsmechanismen en veroorzaakt cellulaire stress wat van invloed kan zijn op het fenotype wat je gaat meten.
les2_opdracht
Maak een experimenteel ontwerp met negatieve en positieve controles voor voorbeeld 5 Voor verdere achtergrondinformatie over controles in CRISPR-Cas9 experimenten klik op de volgende link
Klik voor het antwoord
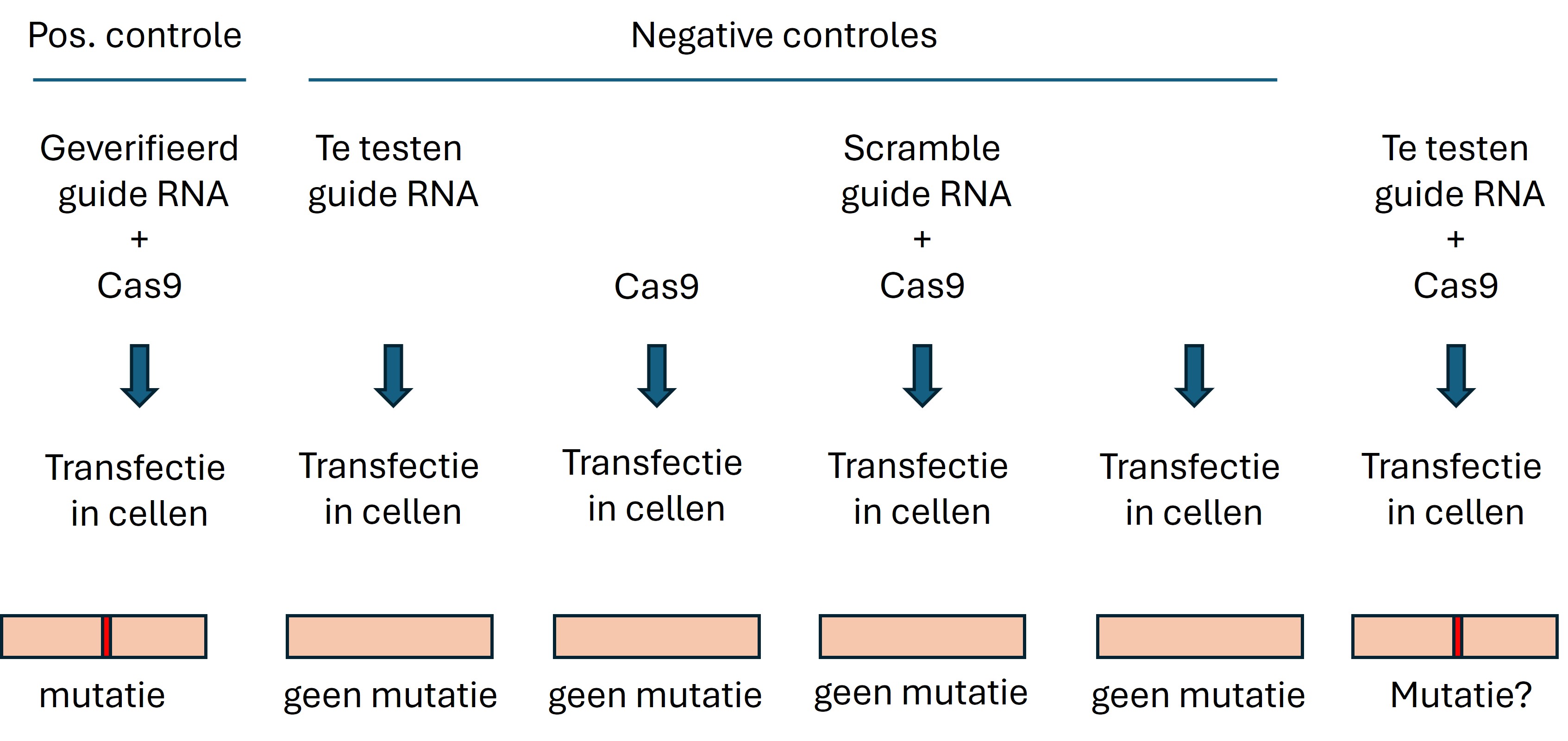
Figure 23: Controles voor een CRISPR-Cas9 experiment
Loading controls
Een loading control is geen experimentele controle, maar een methode voor meetcorrectie. Wanneer je een kwantitatief verschil tussen twee of meerdere experimentele condities wilt bepalen, is het belangrijk om zeker te weten dat het verschil wordt veroorzaakt door de experimentel behandeling en niet doordat er meer cellen (en dus dna, rna en eiwitten) aanwezig waren in de ene experimentele conditie ten opzichte van de andere experimentele conditie. Om voor dit soort variaties te corrigeren, worden de meetwaarden van iedere experimentele conditie genormaliseerd. De meest voorkomende normalisatie methoden in het lab zijn:
- Tellen van het aantal cellen (cell counter)
- Kwantificeren van de hoeveelheid DNA (nanodrop)
- Kwantificeren van de hoeveelheid RNA (nanodrop)
- Kwantificeren van de hoeveelheid eiwit (Bradford, BCA assays)
- Kwantificeren van “house keeping genes” (Western Blot en qRT-PCR)
- Spiking controls. Van te voren wordt in ieder monster dezelfde hoeveelheid van een meetbare stof (spike) toegevoegd. Het doel van een “spike” is om:
- te meten hoeveel er nog van de “spike” aanwezig is na opwerking van een monster. Dit geeft informatie over de recovery; hoeveel materiaal blijft over na opwerking van het monster (recovery)
- de meetwaarde te normaliseren met behulp van de meetwaarden van de “spike”
- als positieve controle. Je weet dat de stof aanwezig is in het monster. Het moet gemeten kunnen worden. Als dit niet het geval is, dan is er een probleem met assay of het meetapparaat (onder de voorwaarde dat de recovery voldoende is; er is nog voldoende van de “spike” over in het monster)
Trouble shooting
Als er geen meetwaarde is in een experiment, inclusief de positieve controle, dan weet je dat er ergens in de uitvoering van het protocol iets mis is gegaan of dat het modelsysteem niet klopt. Maar wat is er misgegaan? Dit kan een lastige vraag zijn om te beantwoorden en is protocol afhankelijk. Je moet dan bij iedere stap in het protocol valideren of deze stap goed is gegaan. Het is daarom zeer belangrijk dat je een goed begrip hebt van alle stappen in een protocol. Bij iedere stap kan je je afvragen wat verwacht ik te zien en kan ik dat tussentijds meten.
Voorbeeld6, klonering:
- Het plasmide en het DNA fragment worden geknipt met twee restrictie enzymen
- Het plasmide en het DNA fragment worden na de restrictie analyse geisoleerd en opgezuiverd
- Het plasmide en het DNA fragment worden in een bepaalde molverhouding samengebracht voor de ligatie reactie
- transformatie van de ligatie reactie in competente bacteriën en uitplaten op selectieve platen
resultaat -> geen kolonies (de klonering is niet gelukt)
Oplossingen:
- De eerste stap is de restrictie van het plasmide en het DNA fragment met twee restrictie enzymen. Als één van de enzymen niet meer actief is kan dat een verklaring zijn waarom de klonering niet gewerkt heeft (het plasmide is wel lineair maar heeft maar één opengeknipte restrictie site). Een technische controle is dan om het plasmide te knippen met de afzondelijke restrictie enzymen zodat je kan testen of beide enzymen actief zijn
- Te weining opbrengst na de zuivering en of de kwalitiet van het DNA is niet voldoende -> nieuwe zuivering
- Gebruik verschillende molverhoudingen van het plasmide en het DNA fragment in de ligatie stap
- Controleer de positieve controle van de transformatie: zijn de E. coli bacterien nog competent genoeg?
Voorbeeld7, Myc overexpressie:
We gebruiken het experiment zoals beschreven in voorbeeld2. Je brengt het MYC oncogen tot overexpressie in HEK293 cellen door middel van een transfectie met een plasmide om het effect op proliferatie te testen (“doubling time). Uit vorige experimenten weet je dat overexpressie van MYC in HEK293 cellen resulteert in lagere”doubling time” (cellen delen sneller). Je wilt dit systeem gebruiken om chemische verbindingen te testen die de activiteit van MYC kunnen remmen. Na transfectie van het plasmide+MYC zie je geen effect op de “doubling time”. Er kunnen verschillende oorzaken zijn:
- De cellen staan al lang in kweek (hoge passage number) en reageren anders dan normaal en of zijn niet meer gezond
- Het plasmide+MYC construct is niet correct
- Het plasmide+MYC construct komt niet in de cel na de transfectie
- Het plasmide+MYC construct komt wel in de cel na de transformatie maar komt misschien niet tot expressie
Oplossingen:
(1) Start een nieuwe batch met HEK293 cellen
(2) Controleer het plasmide door middel van restrictie analyse en of sequencing:
- Misschien heb je het verkeerde plasmide gepakt en of verwisseld
- Misschien heb je het plasmide van een ander lab gekregen en bevat het geen MYC maar een ander gen!
(3) Het plasmide+MYC construct komt niet in de cel na de transfectie:
- controleer de kwaliteit van de plasmide
- optimaliseer de transfectie methode
(4) Controleer het mRNA van cMYC of doe een Western blot analyse om het Myc eiwit aan te tonen. Bij geen resultaat controleer de plasmide (zie oplossing 2)
les2_opdracht
Je werkt met het volgende plasmide om MYC tot overexpressie te brengen in HEK293 cellen. Je wilt het plasmide controlen op de aanwezigheid van de coding sequenctie (CDS) van het MYC gen. Maak een experimenteel ontwerp zodat je kan concluderen of MYC aanwezig is in het plasmide.
Klik voor het antwoord
- Open de plasmide map
- localiseer de positie van de coding sequentie van het MYC gen (2721-1405)
LET OP: het MYC gen is 3’-5’ gepositioneerd (zie figuur 24)
- Ontwerp een sequencing primer voor het MYC gen (~ 100 bp up- of downstream van het MYC gen)
- Stuur plasmide en primer op voor sequencing
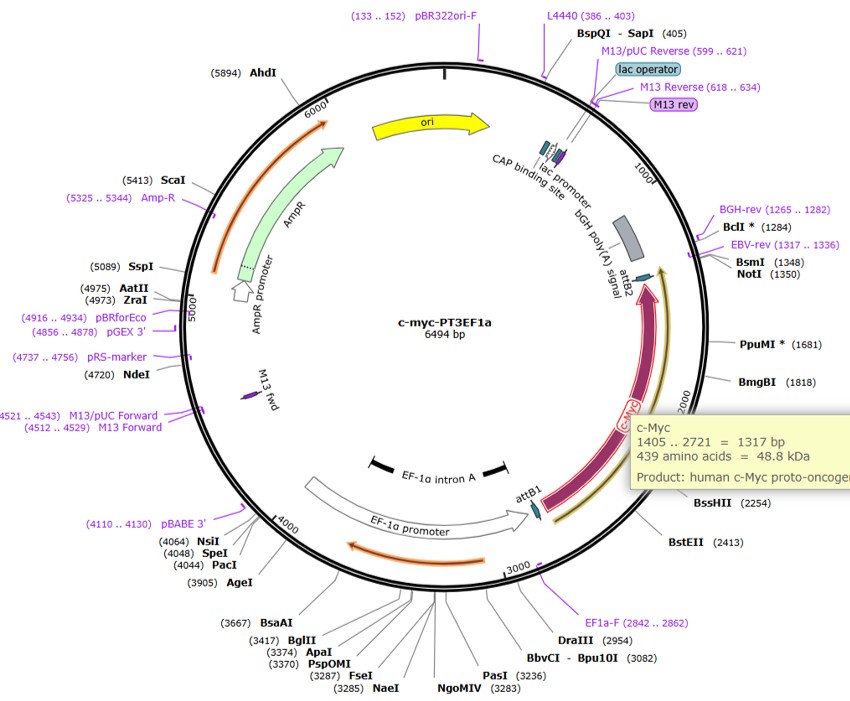
Figure 24: Myc vector map
les2_opdracht
Je wilt MYC tot overexpressie brengen in HEK293 cellen. De plasmide is gecontroleerd en na de transfectie is er geen overexpressie van MYC in de HEK293 cellen. Na het “troubleshooten” is de conclusie dat de transfectie methode niet goed werkt. Het plasmide komt de cel niet in.
Bedenk een assay waarmee je (snel) de transfectie efficiency kan bepalen
Klik voor het antwoord
Je kan gebruik maken van een plasmide die GFP tot expressie brengt. Na de transfectie kan het GFP signaal in de cel snel worden gemeten door een flowcytometer. Op deze manier kan je kwantitatief de transfection efficiency bepalen.
Casus
G-protein coupled receptors (GPCR) spelen een belangrijke rol in de aansturing van biologische processen. Activatie gebeurt door een (natuurlijk) ligand (=first messenger = agonist) waardoor het G-eiwit geactiveerd wordt. Het geactiveerde G-eiwit activeert vervolgens adenylyl cyclase. Dit enzyme maakt cAMP aan wat dient als second messenger voor de activatie van een verscheidenheid aan biologische processen (zie figuur 25).
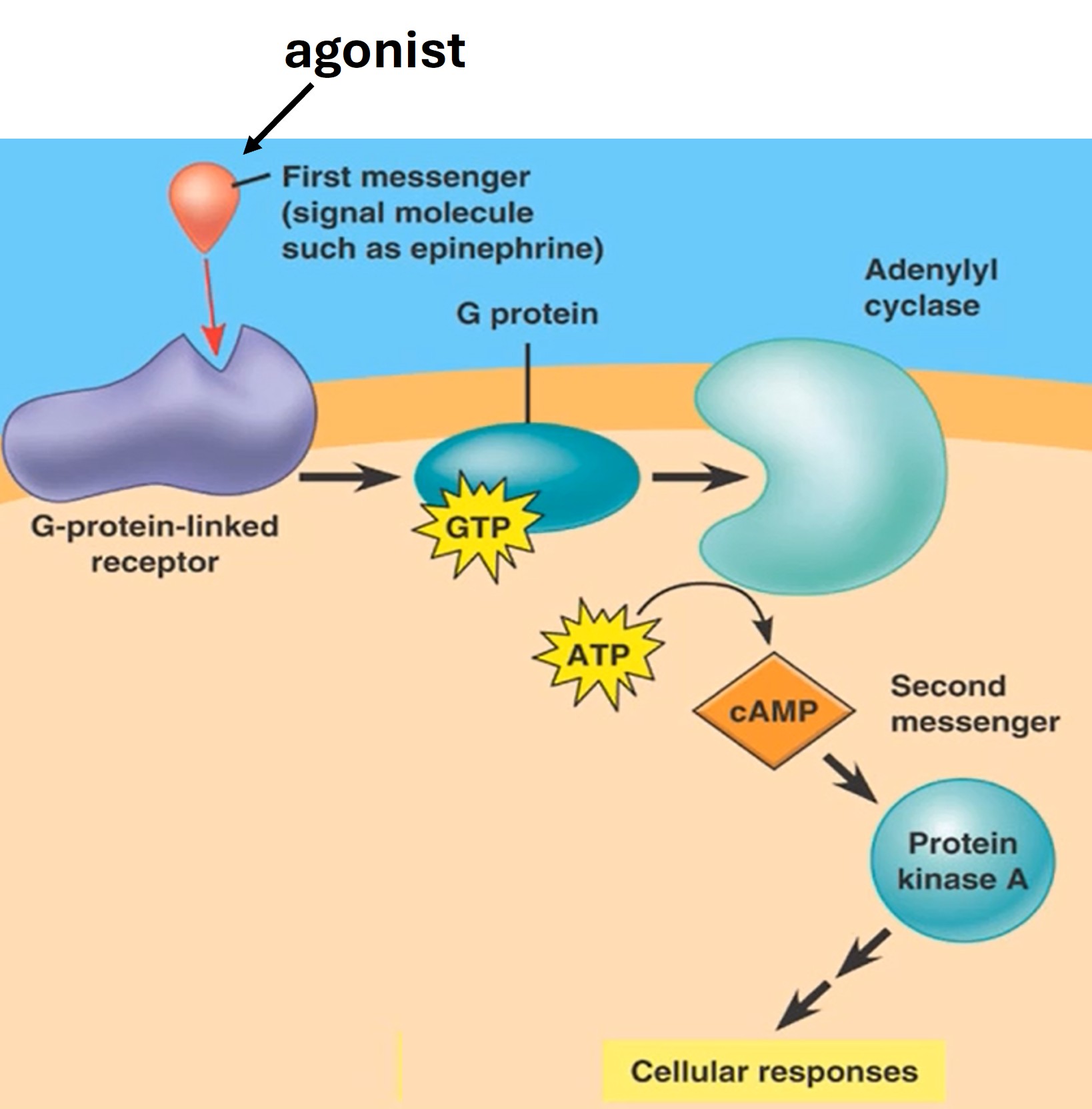
Figure 25: Signaalroute van GCPR
Als deze receptoren te lang geactiveerd worden kan dat resulteren in ziekteverschijnselen. Er is veel interesse om (nieuwe) antagonisten te ontdekken die speficiek de activiteit van GPCR’s remmen. Een voorbeeld zijn beta blockers die de ß1 en ß2 adrenergic receptoren inactiveren.
Om activatie van GPCR te bestuderen wordt onder andere het intracellulaire cAMP gemeten met een biochemische assay. Dit is dus een indirecte maat voor GPCR activatie.
Om potentiele antagonisten te testen moet je werken met cellen waarin de GPCR van interesse aanwezig is en actief wordt na toevoeging van het ligand (zie figuur 26). Als het modelsysteem werkt dan kan je de antagonist toevoegen en testen wat het effect is op de cAMP concentratie in de cellen.
Figure 26: Schema voor experimenteel ontwerp
Er is een nieuw molecuul gesynthetiseerd (Stof X) waarvan gedacht wordt dat het een antagonist is voor een bepaalde GCPR receptor. Maak een experimenteel ontwerp om aan te tonen dat stof X een specifieke antagonist is voor de receptor. Om het ontwerp simpel te houden gebruiken we één concentratie voor de ligand en één concentratie voor de antagonist.
Aanwezig op het lab:
(1) Agonist (activeert de GCPR)
(2) Stof X (antagonist die getest gaat worden)
(3) Bekende (werkende) antagonist
(4) Forskoline (activeert direct adenylyl cyclase)
De werking van de verschillende stoffen wordt weergegeven in figuur 27
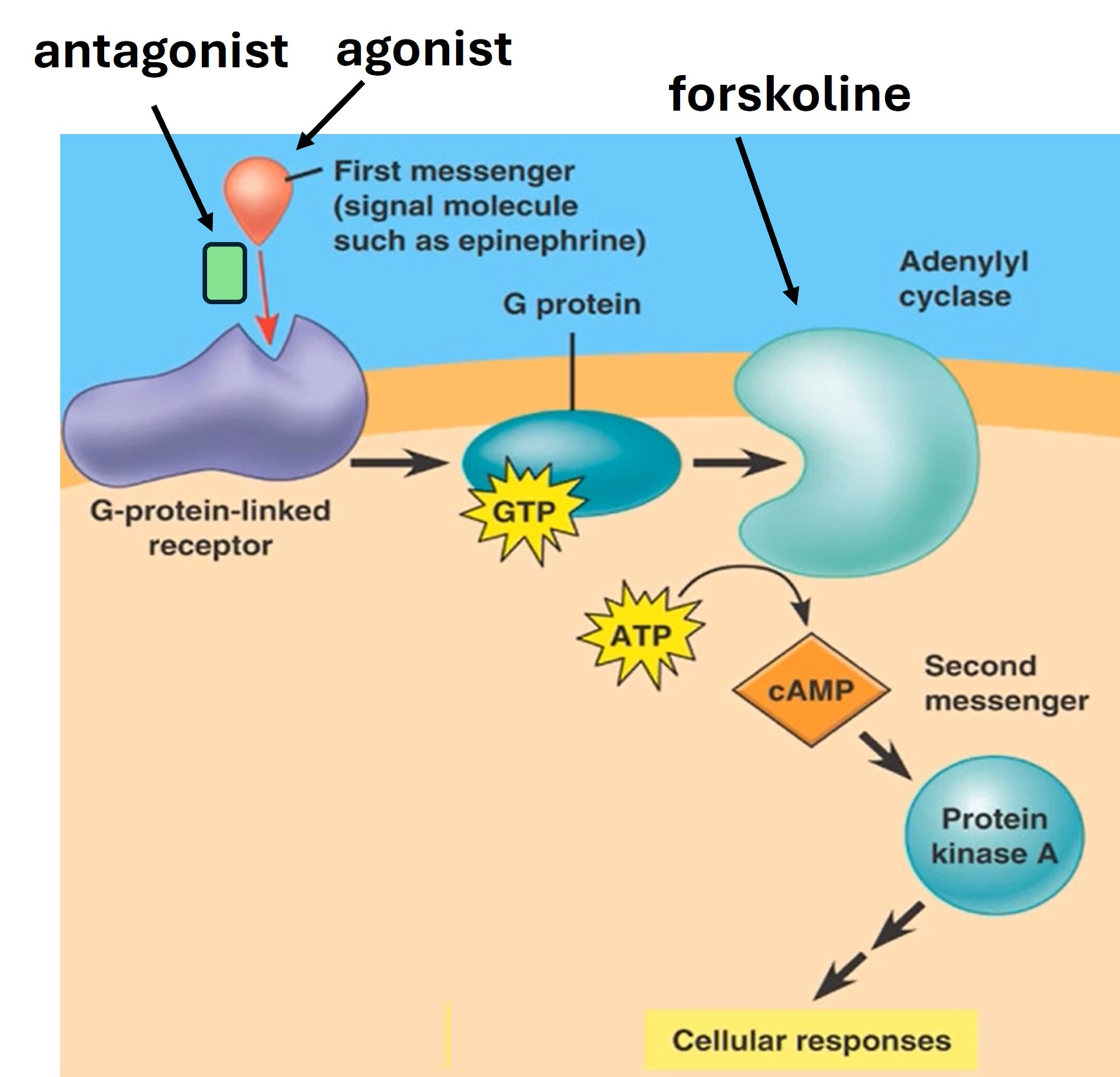
Figure 27: Signaalroute van GCPR + antagonist en forskoline
Welke combinatie van stoffen ga je testen. Wat zijn negatieve, positieve en specificiteits controles?
Geef voor iedere testcondities aan wat je van te voren verwacht!
De uitwerking van deze casus is te vinden in het onderstaande video die opgenomen is door Wouter Nijenhuis. In de video zijn een aantal pauze momenten waarin je moet nadenken over de juiste controles. Neem hiervoor de tijd en ga niet direct door naar de antwoorden!
Uitwerking van casus